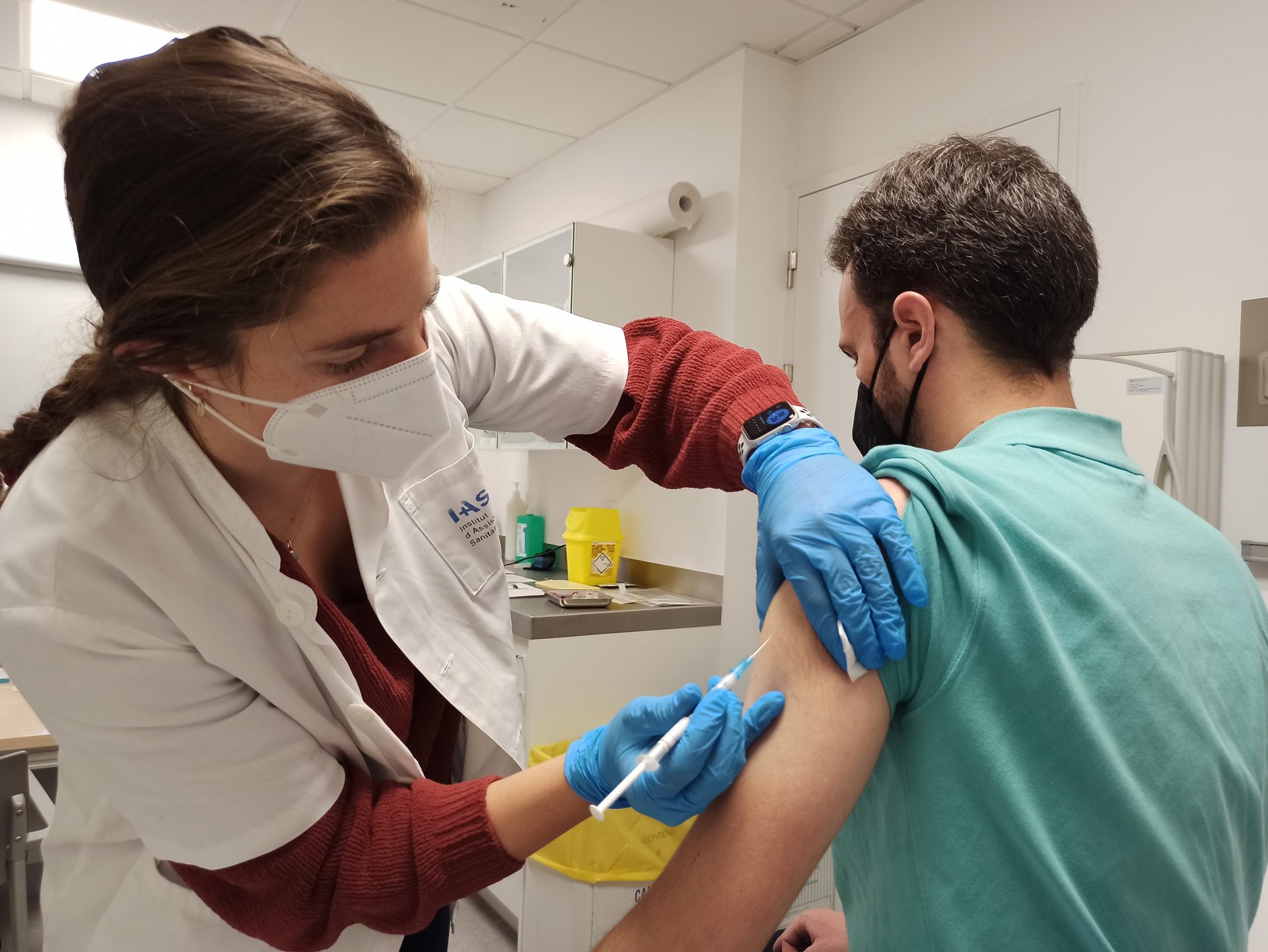
El Hospital Universitario de Girona Josep Trueta esta mañana ha empezado a administrar a los voluntarios de la Fase III la vacuna contra la Covid-19 que está desarrollando la farmacéutica biotecnológica HIPRA. La AEMPS autorizó la semana pasada el ensayo clínico de Fase III, que se inicia una vez que la Fase IIb ha demostrado una buena tolerabilidad, un buen perfil de seguridad y una respuesta potente frente a las variantes, incluida la ómicron. Se trata de la última fase del ensayo clínico antes de la comercialización de la vacuna.
Los primeros voluntarios han sido citados esta mañana en el Hospital Trueta donde, después de realizarles un cuestionario y unas pruebas clínicas, se les ha administrado la vacuna. En esta fase, en total el centro gerundense vacunará a unas 400 personas en dos semanas, a las que se les hará un seguimiento de un año para evaluar la seguridad a largo plazo y la respuesta inmunológica.
En la Fase III, en la que participarán unas 3.000 personas mayores de 16 años y que tendrá lugar en 17 hospitales de España, 2 de Portugal y 1 de Italia, se continuará evaluando la seguridad y eficacia de la dosis de refuerzo de la vacuna de HIPRA contra la Covid-19 en un grupo mayor de personas vacunadas con diferentes vacunas (AstraZeneca, Moderna, Pfizer y Janssen). En este estudio se quiere confirmar que la inmunización de refuerzo con la vacuna de HIPRA puede ampliar la protección frente a las nuevas variantes y prolongar el efecto preventivo de la vacunación.
Las personas que participen en el ensayo deben haber recibido una o dos dosis de una de las vacunas autorizadas (Comirnaty (Pfizer), Spikevax (Moderna), Vachevria (AstraZeneca), Janssen (Janssen) o combinadas) como mínimo hace 3 meses. En la casuística que hayan pasado la Covid-19 al menos hace 1 mes, sin haber ingresado en el hospital, podrán participar igualmente en el estudio. Cada hospital ha habilitado un espacio en su web para que las personas interesadas puedan inscribirse.
La vacuna de HIPRA
La vacuna contra la Covid-19 de HIPRA es una vacuna de proteína recombinante multivariante adyuvada, basada en un heterodímero de fusión del dominio de unión al receptor (RBD) que contiene las variantes B.1.1.7 (alfa) y B.1.351 (beta) del SARS-CoV-2.
La vacuna de HIPRA se conserva a temperatura de refrigerador (entre 2 y 8 ºC), facilitando el almacenamiento y distribución. Sin embargo, la tecnología utilizada permite una gran versatilidad para adaptarla a nuevas variantes del virus, si fuera necesario en el futuro. Los resultados obtenidos a fecha de hoy, muestran que la vacuna produce anticuerpos neutralizantes frente a las VOC (variantes de “preocupación”) actuales y también eficacia en la prevención de la enfermedad.
20 hospitales participan en la Fase III
En la Fase III de la vacuna de HIPRA participan diferentes hospitales públicos y privados ubicados en España (17), Portugal (2) e Italia (1): en Cataluña, además del Hospital Universitario de Girona Josep Trueta, también participan el Hospital Germans Trias i Pujol; Hospital Clínico de Barcelona; Hospital Vall d'Hebron Barcelona Hospital Campus Hospital de Mollet, Hospital HM Nuevo Delfos Barcelona y Hospital Quironsalud Barcelona; además, el de la Comunidad de Madrid participa el Hospital Universitario La Paz (Madrid); Hospital Universitario Príncipe de Asturias (Alcalá de Henares); Hospital General Universitario Gregorio Marañón (Madrid); Hospital Universitario HM Montepríncipe (Madrid); Hospital Universitario HM Sanchinarro (Madrid); Hospital Universitario HM Puerta del Sur (Móstoles); Hospital Universitario Quironsalud Madrid (Madrid); además del Hospital Universitario de Cruces (Barakaldo, Euskadi); Hospital Regional Universitario de Málaga (Málaga, Andalucía); Hospital Clínico Universitario de Valencia (Valencia, Comunidad Valenciana); Hospital Univ. Minho Braga (Braga, Portugal); Hospital Algarve Biomedical Center (Algarve, Portugal); Hospital Niguarda (Milano, Italia).
El ensayo clínico de la vacuna de HIPRA se lleva a cabo por dos equipos de investigación, con tres investigadores principales. Uno de ellos es el Grupo de Epidemiología en Salud Vascular del Institut Català de la Salut en Girona liderado por el Dr. Rafel Ramos ―investigador del Instituto Universitario de Investigación en Atención Primaria (IDIAP) Jordi Gol y del Instituto de Investigación Biomédica de Girona Dr. Josep Trueta (IDIBGI). Por otro lado, en el Hospital Clínic de Barcelona está trabajando un equipo multidisciplinar de profesionales médicos, de enfermería y administración de los servicios de Enfermedades infecciosas y del Servicio de Medicina preventiva y epidemiología.